
A importância dos Estudos Clínicos comparativos nos Ensaios Farmacocinéticos
por Allcrom
Um artigo de Hugues Chanteux e outros pesquisadores (da UCB Biopharma Belgium e duas outras instituições) publicado na edição de novembro de 2023 do The AAPS Journal descreveu o uso de Dispositivos de Microamostragem Mitra® baseados na Tecnologia VAMS® em vários ensaios clínicos para o desenvolvimento de um anticonvulsivante chamado Padsevonil (PSL). Seu artigo foi intitulado “Estudos clínicos comparativos e abordagem de modelagem para implementação de uma técnica de amostragem centrada no paciente no desenvolvimento clínico do Padsevonil.”
O grupo de pesquisa realizou um extenso estudo clínico de comparativo (bridging study) envolvendo mais de 2.500 amostras de Sangue pareadas de pacientes com epilepsia e voluntários saudáveis.
A partir de seu trabalho, eles puderam concluir que a abordagem usada para o estudo comparativo foi considerada adequada pela Food and Drug Administration (FDA) para apoiar os Dispositivos Mitra® como o único método para amostragem Farmacocinética (PK) em futuros ensaios clínicos.
Amostras de Plasma Versus Amostras de Sangue Total
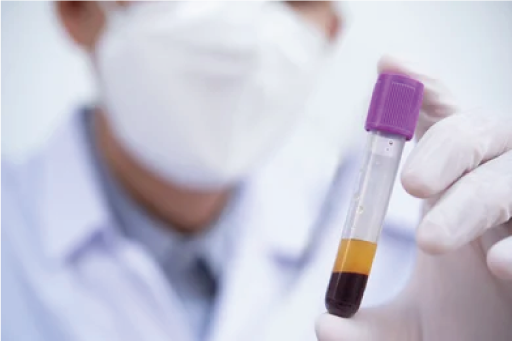
Tradicionalmente, a matriz biológica padrão-ouro para medir a concentração de drogas no Sangue é o Plasma. O Plasma é o líquido cor de palha que permanece quando a porção celular intacta do Sangue (Hematócrito ou Ht) é removida por centrifugação ou filtração.
Há boas razões pelas quais os medicamentos são tradicionalmente analisados a partir do Plasma e não do Sangue total.
Uma razão é que o Plasma é uma matriz menos complexa, portanto, há menos interferências de matriz para mitigar ao quantificar as concentrações de moléculas de fármaco. Isto é particularmente importante para aplicações LC-MS onde os efeitos de intensificação e supressão de matriz são comumente observados e precisam ser controlados.
Outra razão é que as Drogas livres de Proteínas no Plasma são muitas vezes o que está disponível para as células periféricas interagirem, permitindo efeitos farmacológicos. Como resultado, é útil medir a mudança nas concentrações de fármacos livres durante os estudos farmacocinéticos.
No entanto, o Plasma não é isento de desvantagens. Em primeiro lugar, um ensaio de Plasma não leva em conta qualquer partição que o fármaco tenha realizado no Hematócrito. Isso é importante com medicamentos que se dividem preferencialmente
no Ht, onde a remoção do Ht resultará na remoção da maior parte do medicamento. Há um risco de sub-representar a concentração do fármaco em estudos de fármacos à base de Plasma.
Nessas circunstâncias, medir a concentração do fármaco a partir do Sangue total, que contém células, é vital para obter uma concentração representativa. Um exemplo de tal classe de medicamentos que se associam principalmente com o Ht são os inibidores de Calcineurina, tais como Tacrolimus e Ciclosporina.
Para a grande maioria dos fármacos, a molécula se divide igualmente no Ht ou o particionamento favorece a fração plasmática. É por isso que o Plasma tem sido historicamente a matriz preferida para medir os níveis de concentração do fármaco para uma variedade de medicamentos. Devido as melhorias na tecnologia analítica, é possível medir esses medicamentos a partir do Sangue total também.
Por Que o Estudo Clínico Comparativo?
No entanto, se um ensaio foi inicialmente validado no Plasma venoso, então o comparativo clínico precisa ser realizado para entender quais vieses são vistos ao fazer a transição para o Sangue total. Em primeiro lugar, o particionamento entre Sangue total e Plasma (B:P) pode ser dinâmico. Nessas circunstâncias, o particionamento pode ser dependente da concentração e/ou do tempo. Além disso, as concentrações de fármaco podem não ser as mesmas na circulação periférica em comparação com a circulação central como amostradas no Sangue venoso.
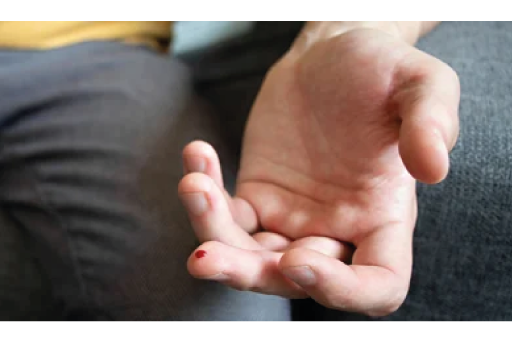
Portanto, é importante verificar se há diferenças na concentração do medicamento quando se trata do local da coleta (por exemplo, ponta do dedo vs. braço).
Finalmente, o impacto dos anticoagulantes precisa ser levado em consideração quando o Sangue capilar não coagulado é coletado e comparado ao Plasma venoso coletado do Sangue estabilizado.
Conforme discutido no artigo resumido aqui, a equipe da UCB Biopharma na Bélgica usou Dispositivos Mitra® baseados na Tecnologia VAMS® em várias fases de ensaios clínicos durante o desenvolvimento do fármaco do anticonvulsivante Padsevonil (PSL). Os Dispositivos Mitra® ofereceram às suas coortes de estudo uma amostragem remota conveniente, permitindo a coleta de < 30 µL de amostras de Sangue em casa a partir de uma punção digital. As amostras remotas puderam ser coletadas pelas próprias coortes do estudo ou com a ajuda de um amigo ou membro da família.
Os Dispositivos Mitra® forneceram amostras de Sangue seco para análise, o que foi um benefício, porque o Sangue seco é muitas vezes considerado mais seguro e mais estável do que o Sangue líquido. Por esse motivo, as amostras de Sangue seco geralmente podem ser enviadas para testes nos laboratórios através do serviço de postagem tradicional, o que elimina a necessidade de transporte e armazenamento em cadeia fria. Esses benefícios tornam a microamostragem volumétrica absorvente ideal para grandes ensaios clínicos multicêntricos.
Foi fundamental para a equipe da UCB Biopharma entender completamente a cinética de particionamento do medicamento do Sangue para o Plasma, conduzindo um extenso comparativo clínico. A partir desses dados, eles foram capazes de desenvolver um algoritmo para compensar o particionamento dinâmico de B:P que observaram.
Resultados do Estudo de Particionamento de Sangue Total e Plasma em Ensaios Farmacocinéticos
Seis ensaios clínicos foram conduzidos para entender a PK do PSL, onde a análise da relação entre as amostras Mitra® e Plasma venoso foi investigada. Quatro desses ensaios foram empregados para o desenvolvimento do método e os dois últimos (que incluíram um ensaio de fase 2) para validação do método.
- Os participantes do estudo eram de uma mistura de origens e etnias e dependentes do ensaio clínico, as coortes eram pacientes ou voluntários saudáveis.
- No total, 3.048 amostras pareadas foram coletadas e analisadas.
- O extenso trabalho comparativo foi conduzido para apoiar a aprovação regulatória de um estudo de fases 2b/3 em que a amostragem PK foi conduzida exclusivamente com Dispositivos Mitra®.
- Embora o programa de desenvolvimento de medicamentos tenha sido interrompido por razões não relacionadas ao estudo comparativo, o grupo disse que “a presente estratégia comparativa foi compartilhada durante uma interação Tipo C e foi considerada adequada pela FDA para apoiar o uso do Mitra® como abordagem única de amostragem farmacocinética em futuros ensaios clínicos”.
- Um efeito de tempo na razão B:P foi observado, onde eles viram um aumento após a dosagem de 0,5 a 2 horas e isso caiu para seu valor de estado estacionário após cerca de 4 horas.
- Outros estudos observaram que a razão pré-dose B:P foi semelhante ao valor do estado estacionário de 4 horas.
- O grupo disse que isso poderia ser explicado pelos diferentes locais de amostragem dos quais o Sangue foi coletado.
- O Sangue da coleta por punção digital é de consistência diferente em comparação com o Sangue obtido da coleta venosa. O grupo UCB Biopharma comentou que o Sangue coletado por punção digital é uma mistura de Sangue principalmente arteriolar, venoso e capilar, em vez do que classicamente consideraríamos como Sangue capilar. Eles explicaram que, nos estágios iniciais de medição farmacocinética, essa concentração sanguínea arterial pode ser maior do que a concentração venosa, devido à extração eficiente de Drogas das arteríolas para o tecido. Assim, durante essa etapa de distribuição, ela pode levar a um aparente maior B:P. Esse fenômeno também foi descrito em outros estudos citados por eles.
- Eles desenvolveram um modelo de efeito misto linear com base em estudos de farmacologia clínica. Usando este e outros dados, eles foram capazes de prever adequadamente o Plasma das amostras Mitra® com um viés médio de <9%.
- O B:P in vivo espelhou os dados in vitro.
Conclusões dos Autores do Estudo
O artigo destaca a importância do comparativo clínico para correlacionar amostras de Sangue coletadas por punção digital e Sangue venoso coletado de uma veia do braço.
- A abordagem foi considerada adequada pela FDA para estudos de amostragem farmacocinética usando apenas amostras de Sangue seco Mitra®.
- O trabalho estabelece as bases para a implementação do comparativo para estudos futuros.
Para mais informações entre em contato com [email protected]
Comentários da Neoteryx Microsampling por Trajan
O trabalho resumido aqui mostra a implementação bem-sucedida do uso de amostras de Sangue seco em um programa de desenvolvimento de medicamentos, onde mais de 2.500 amostras pareadas foram coletadas com sucesso. Os dados do comparativo clínico demonstraram que era possível usar apenas amostras de Sangue seco para parte do estudo. O trabalho também mostrou que ambas as amostras coletadas na clínica e remotamente poderiam ser efetivamente correlacionadas.
Além disso, este estudo destacou a importância do local de amostragem (ou seja, ponta do dedo versus braço) e como a concentração da Droga pode mudar entre o Sangue venoso e o Sangue capilar coletado de um dedo, especialmente nos estágios iniciais da dosagem. Compreender esse fenômeno e mitigá-lo usando modelos estatísticos de pontes clínicas aumenta a probabilidade de uso bem-sucedido de amostras de Sangue seco em futuros ensaios clínicos remotos ou híbridos.
Os leitores são encorajados a consultar um excelente artigo de Rowland e Emmons, que discute em profundidade o impacto do uso de Sangue seco em estudos de farmacocinética (um ponto que também foi destacado pelos autores deste estudo).
Para mais informações entre em contato com [email protected]

